Общая характеристика риккетсий и риккетсиозов
Общие вопросы химиопрофилактики и химиотерапии риккетсиозов
Многолетний эмпирический опыт терапии больных риккетсиозами антибиотиками различных классов в последние годы сочетается с определением чувствительности возбудителей к препаратам in vitro, в том числе на системе различных культур клеток или РКЭ (Плеханова Т. М. и др., 1998; Maurin et Raoult, 1997; Rolain et al, 1999). В результате установлено следующее. Наиболее эффективными и коммерчески доступными средствами этиотропной терапии риккетсиозов являются препараты группы тетрациклинов и фторхинолонов. В клинической практике целесообразно использование полусинтетического производного окситетрациклина — доксициклина. Сохраняя широкий спектр антибактериальной активности, он обладает наилучшими фармакокинетическими характеристиками, в частности, по периоду полувыведения: для доксициклина этот период составляет 16-24 часа против 12-16 для миноциклина и 6-14 для других препаратов из группы тетрациклинов (Белоусов Ю. Б. и др., 1993).
Исследованиями Winker H. и Daugherty R. (1989) на модели сыпнотифозной инфекции в культуре клеток установлено, что тетрациклин и хлорамфеникол останавливают синтез протеинов риккетсий и, соответственно, их рост путем ингибирования фосфолипазы А2 микроорганизма. Происходит блокирование начальной фазы инфекционного процесса на стадии прикрепления и внедрения риккетсий в чувствительную клетку-мишень. Снижение фосфолипазной активности наблюдается очень быстро, уже спустя 4 ч после добавления антибиотика в инфицированную культуру клеток. Для достижения равного эффекта подавления роста риккетсий требовалась большая, примерно в 2,5 раза концентрация хлорамфеникола, в сравнении с тетрациклином. Кроме того, продемонстрировано, что доксициклину, помимо этиотропного влияния, свойственно и патогенетическое действие, так как препарат также подавляет синтез производных азотной кислоты в зараженных риккетсиями клетками и тем самым оказывает противовоспалительный эффект (Agostino et al., 1998).
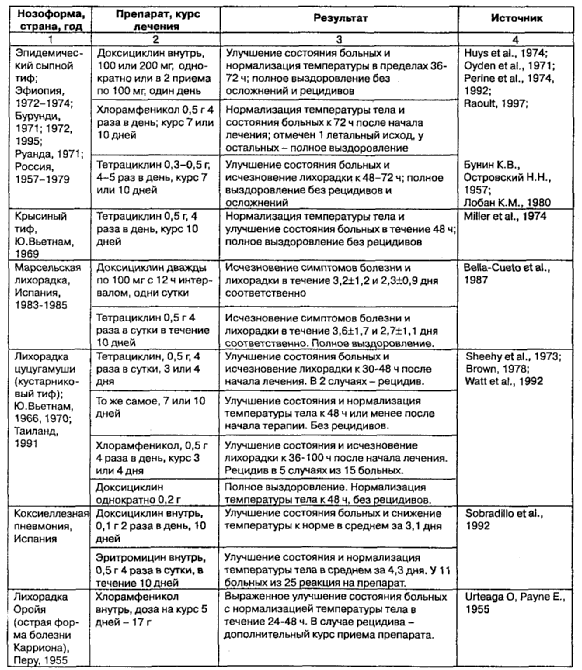
Таблица 6
Пенициллин, наоборот, не оказывает какого-либо влияния на фосфолипазную активность риккетсий.
Назначение тетрациклина или доксициклина в общетерапевтических дозах (2,0 г тетрациклина или 200 мг доксициклина в сутки для взрослого) при острых формах риккетсиозов, таких как эпидемический и крысиный сыпной тиф, марсельская лихорадка, лихорадка цу-цугамуши (табл. 6), японская пятнистая лихорадка и моноцитарный эрлихиоз быстро, в течение 24-72 ч, улучшает состояние больных и, соответственно, приводит к нормализации температуры тела к 36-96 ч после начала лечения с последующим полным выздоровлением. По сути дела, лечение острых риккетсиозов может быть сведено лишь к приему доксициклина (200 мг в 2 капсулах), как это и было рекомендовано ВОЗ при ликвидации большой вспышки сыпного тифа в Бурунди в 1997 году. Очевидно также, что доксициклин имеет преимущество в сравнении с другими препаратами вследствие простоты применения и невысокой стоимости при равной эффективности. Для лечения пятнистых лихорадок у детей и беременных может быть использован и джозамицин (препарат из группы макролидов), поскольку его токсичность крайне низка (Drancourt, Raoult, 1993). Широкодоступные пенициллины, хлорамфеникол, котримоксазол и некоторые макролиды (эритромицин, олетерин), хотя и проявили некоторую эффективность при лечении отдельных нозоформ, все же уступают тетрациклинам, не обеспечивая ожидаемого результата.
На примере наиболее злокачественного риккетсиоза с выраженной природной очаговостью, а именно пятнистой лихорадки Скалистых гор (ПЛСГ), наглядно прослеживается прямая связь между исходом болезни и использованным средством лечения. Если в 1935-1956 гг., т.е. до внедрения в клиническую практику препаратов, действующих на грамотрицательную микрофлору, летальность при этой инфекции составляла 22%, то в последующие годы благодаря терапии тетрациклином и хлорамфениколом, она снизилась до 3,0-7,5% (Smadel, 1959; Dalton et al., 1994), хотя и сохранялась в отдельных штатах на уровне 13%(KirklandetaL, 1992).
Риск гибели прямо коррелировал с возрастом заболевших, видом применяемого антибиотика и сроком начала специфического лечения (Krebs et al., 1994). Запоздалое назначение препарата (позднее 2-5-го дня от начала болезни) чаще всего было обусловлено ошибками в первоначальном диагнозе, вследствие атипичной клинической картины заболевания из-за отсутствия сыпи у больных (57% случаев) в момент их первого обращения к врачу и отсутствия в анамнезе указания на контакт с клещом (до 50%). Нередкое отсутствие одного из указанных кардинального для ПЛГС признака или отсутствие их обоих одновременно затрудняло диагноз болезни и, соответственно, явилось причиной задержки специфического лечения (Kirkland et al., 1992).
Кроме того, из сопоставления результатов терапии ПЛГС хлорам-фениколом и тетрациклином следует, что в группе больных, получавших лечение хлорамфениколом, летальность на 827 наблюдений составила 8,9%, тогда как в группе, леченной тетрациклином, она не превышала 1,6% на 2256 больных (Dalton et al., 1994).
Очевидно, что при подозрении на риккетсиозную этиологию лихорадочного заболевания, особенно такого как ПЛГС, лихорадка цуцугамуши, марсельская лихорадка и коксиеллез, лечение антибиотиками широкого спектра действия (тетрациклин, доксициклин, миноциклин, рифампицин) должно быть немедленным, особенно у лиц старшего возраста и ослабленных больных. При назначении антибиотиков следует также учесть то, что такая терапия при своевременном применении в первые дни болезни, по существу, является этиотропной и патогенетической одновременно; это приводит к задержке специфического антительного ответа у больного и к продукции антител на невысоком уровне, иногда ниже диагностических значений (Gray et al., 1990). Но в этом случае быстрый эффект терапии следует расценивать как косвенное доказательство риккетсиозной этиологии болезни.
Наиболее сложную и трудную проблему представляет терапия коксиеллеза и хронических форм бартонеллезов. Лечение, в частности, эндокардитов коксиеллезной этиологии и других более редких осложнений лихорадки Ку, а также хронических форм бартонеллезов остается сложным и требует настойчивой, зачастую многомесячной, комбинированной терапии. Если химиопрепарат не проникает внутрь клеток, в которых паразитирует возбудитель и не аккумулируется внутри фаголизосомы (а именно в них «укрываются» коксиеллы), то он становится неэффективным и его применение малорезультативно. Вероятно, по этой причине часть препаратов группы макролидов и аминог-ликозидов (гентамицин, эритромицин, ванкомицин), а также новые антибиотики группы фторхинолонов (норфлоксацин, пефлоксацин), характеризующиеся относительно быстрым (менее 8-10 ч) периодом полувыведения из организма человека, оказываются недостаточно эффективными для лечения коксиеллеза. Так, в сравнительном исследовании результатов терапии 111 случаев острой лихорадки Ку, протекающей в различных клинических формах, свойственной этому заболеванию (см. главу: лихорадка Ку), Spelman et al. (1982) установили, что применение в общетерапевтических дозах тетрациклина (500 мг, 4 раза в день) в течение двух недель и доксициклина (100 мг дважды в день) в течение такого же срока привело к быстрому клиническому излечению всех больных. Средняя продолжительность лихорадки после начала терапии составила 2,0 и 1,7 дня соответственно. Однако в одном случае лечения тетрациклином, одном случае терапии доксициклином у 3 больных с выявленным коксиеллезным эндокардитом полного излечения не произошло. Выздоровление этих больных наступило лишь после дальнейшего длительного приема антибиотика. Кроме того, у 425 больных развилась посткоксиеллезная астения, и часть больных этой группы получила второй дополнительный курс лечения доксициклином. Именно поэтому авторы отдают предпочтение доксициклину и рекомендовали расширить основной первоначальный курс лечения данным антибиотиком до 4 недель (Spelman et al., 1982).
Аналогичной тактики пролонгированной (не менее 21 дня) терапии доксициклином при лечении острой лихорадки Ку придерживаются и французские авторы (Musso, Raoult, 1995). По результатам терапии острой (178 наблюдений) и хронической (71 больной) лихорадки Ку, осуществляемой хлорамфениколом, макролидами, доксициклином и хинолонами, под контролем присутствия коксиелл в крови и в биопробах из пораженных тканей, авторы заключили, что укороченный курс лечения антибиотиком является клинически эффективным в отношении острой лихорадки Ку, но не приводит к освобождению организма больного от коксиелл и, следовательно, не предупреждает возможную эволюцию к хронической форме болезни. Поэтому лечение должно проводиться достаточно длительно, и в наблюдениях последних авторов терапия доксициклином продолжалась в течение трех недель для острой лихорадки Ку. Терапия же хронических форм проводилась значительно продолжительнее, настойчиво — от одного-двух месяцев до полугода и более, с ежедневным приемом комбинаций антибиотиков: доксициклин с хинолонами, доксициклин с гидрооксих-лороквином, доксициклин в сочетании с рифампицином. Эффективность лечения периодически контролировали высевами коксиелл из крови или из биоптатов тканей (Musso, Raoult, 1995). Имеются также сообщения о высокоэффективном лечении легочной формы лихорадки Ку фторхинолонами при отсутствии осложнений (Bestland et al., 1988).
Лечение эрлихиозов, независимо от видовой принадлежности возбудителя, успешно осуществляется доксициклином (Walker D., 1996). Оценка чувствительности возбудителя моноцитарного эрлихиоза человека, Е. chaffeensis, к различным антибиотикам подтвердила необоснованность эмпирического применения хлорамфеникола и, наоборот, перспективность назначения рифампицина, особенно при лечении эрлихиоза у детей и у женщин в период беременности. Минимальная ингибирующая рост эрлихий в культуре клеток концентрация доксициклина и рифампицина была менее чем 0,5 и 0,125 мг/мл соответственно, тогда как хлорамфеникол не задерживал развитие возбудителя даже при концентрации антибиотика выше 16 мг/мл (Brouqui, Raoult, 1992).
Гранулоцитарный эрлихиоз успешно излечивается тетрациклинами с возвращенияем температуры и клинического состояния больных к норме в течение 24-28 ч после приема препарата (Bakken et al., 1996).
Систематизированные данные по лечению бартонеллезов отсутствуют, либо их терапия проводилась эмпирически неадекватным химио-препаратом. Рационально обоснованная терапия этой группы заболеваний, по-видимому, должна быть основана на данных Maurin et al. (1993,1996), а также Rolainet al. (1999). Определяя чувствительность бартонелл всех видов, патогенных для человека, к антибиотикам различных классов in vitro, авторы показали, что все изоляты бартонелл были высокочувствительны к беталактамам, аминогликозидам, макролидам, тетрациклинам и рифампицину. Минимальная концентрация, подавляющая рост 90% бактерий (МП К») по отношению, например, к В. guintana, была равна 0,06-0,12 мг/мл для азитромицина, доксициклина, рифампицина и спарфлоксацина (Maurin etal., 1995). Подтвержден универсальный характер действия тетрациклинов, эритромицина, рифампицина, а также беталактамов в отношении возбудителей всех бартонеллезов. При этом отмечена широкая вариация в дозах, подавляющих рост бактерий или оказывающих бактерицидное действие (Maurin et al., 1995; Rolain et al., 1999).
Поразительный эффект своевременного применения этиотропной терапии наблюдали при лечении болезни Кариона в ее острой форме (лихорадка Оройя) в одном из отдаленных поселений в Перу, в эндемичном очаге инфекции. Прием хлорамфеникола (иные препараты отсутствовали) предупредил фатальные исходы у всех больных, получивших лечение антибиотиком, при гибели 14 из 16 заболевших, не получивших препарат (Gray et al., 1990).
Из ограниченного опыта лечения хронических форм бартонеллезов, в частности, бациллярного ангиоматоза и рецидивирующих лихорадочных состояний, обусловленных либо В. quintana, В. henselae, видно, что лечение становится успешным при длительном и настойчивом применении в течение нескольких месяцев комбинированной терапии: ципрофлоксацин (750 мг внутрь ежедневно) и рифампицин (900 мг ежедневно) до полной элиминации возбудителя из организма больных (Luccy et al., 1992; Colson et al., 1996). Совершенно очевидно, что при терапии бартонеллезов имеет значение не столько выбор антибиотика, сколько продолжительность курса лечения (Maurin et al., 1996) и выбор наиболее рациональной комбинации антибиотиков группы тетрациклинов и аминогликозидов. В частности, применение гентамицина в сочетании с доксициклином не менее чем в течение 6 недель должно защитить от бартонеллезных эндокардитов (Rolain et al., 1999).
Само собой разумеется, что этиотропная терапия антибиотиками должна быть подкреплена патогенетическими препаратами с учетом клинического состояния больного.
В заключение необходимо обратить внимание на то обстоятельство, что некоторыми французскими (Herreman, 1966; Giroud, Capponi, 1968), румынскими (Илиеску К. и др., 1962; Nicolau, Constantinescu, 1965; Стоя И. и др., 1965) и турецкими исследователями (Payzin, Akan, 1966) высказывалось предположение о возможности не только длительного паразитирования риккетсий в организме переболевших, но и о возможности развития в связи с этим у них различного рода сердечной и сосудистой патологии через многие годы после перенесенного риккетсиоза. Это детерминируется ангиотропизмом в паразитировании риккетсий, который патогистологически проявляется в виде сосудистого эндотелиоза, а в остром периоде риккетсиоза — в виде специфического риккетсиозного гранулематоза. Риккетсиям приписывается ответственность за возможность последующего развития у перенесших основной процесс миокардиокоронаритов, тромбангиитов и даже инфаркта миокарда.
Указанные выше французские и румынские исследователи считают, что такая патология может быть обусловлена риккетсиями Провачека, риккетсиями Музера, риккетсиями Конора и коксиеллами Бернета. Такого рода суждения обосновываются тем, что у больных с сердечно-сосудистой патологией иногда выявляются антитела в сыворотке крови больных к риккетсиям и даже, возможно, выделение самих риккетсий. Больше это касается коксиелл Бернета, которые являются, пожалуй, единственным видом риккетсий, способным вызывать тяжелую патологию сердца у больных лихорадкой Ку, причем не только по типу интерстициального миокардита, но даже и риккетсиозный эндокардит. Последний описан у ряда больных и, как правило, характеризуется затяжным или даже хроническим течением. Затяжное течение болезни, не свойственное другим риккетсиозам, при лихорадке Ку объясняется размножением и развитием риккетсий в гистиоцитах, а затем и в макрофагах органов (макрофагальной) ретикуло-эндотелиальной системы, в то время как при других риккетсиозах возбудители паразитируют в основном в эндотелии сосудов. Захваченные лейкоцитами, макрофагами и гистиоцитами, коксиеллы Бернета частично лизируются (в основном в лейкоцитах), но могут также и размножаться в них. Речь идет, таким образом, о том, что фагоцитоз риккетсий при лихорадке Ку имеет, в отличие от других риккетсиозов, незавершенный характер. С этим, повидимому, и следует связывать наличие субклинических форм болезни и латентно протекающей инфекции при данном риккетсиозе.
Именно латентная инфекция в последующем, по представлению указанных выше авторов, и может вести к медленному прогрессирующему процессу с развитием картины коронарита, миокардиокоронарита и ишемии миокарда. Выявление в сыворотке крови комплемент-фиксирующих антител к риккетсиям может быть косвенным подтверждением гипотезы о причастности риккетсий к патологии сердечно-сосудистой системы у переболевших когда-то лихорадкой Ку или другими риккетсиозами.
Многолетний эмпирический опыт терапии больных риккетсиозами антибиотиками различных классов в последние годы сочетается с определением чувствительности возбудителей к препаратам in vitro, в том числе на системе различных культур клеток или РКЭ (Плеханова Т. М. и др., 1998; Maurin et Raoult, 1997; Rolain et al, 1999). В результате установлено следующее. Наиболее эффективными и коммерчески доступными средствами этиотропной терапии риккетсиозов являются препараты группы тетрациклинов и фторхинолонов. В клинической практике целесообразно использование полусинтетического производного окситетрациклина — доксициклина. Сохраняя широкий спектр антибактериальной активности, он обладает наилучшими фармакокинетическими характеристиками, в частности, по периоду полувыведения: для доксициклина этот период составляет 16-24 часа против 12-16 для миноциклина и 6-14 для других препаратов из группы тетрациклинов (Белоусов Ю. Б. и др., 1993).
Исследованиями Winker H. и Daugherty R. (1989) на модели сыпнотифозной инфекции в культуре клеток установлено, что тетрациклин и хлорамфеникол останавливают синтез протеинов риккетсий и, соответственно, их рост путем ингибирования фосфолипазы А2 микроорганизма. Происходит блокирование начальной фазы инфекционного процесса на стадии прикрепления и внедрения риккетсий в чувствительную клетку-мишень. Снижение фосфолипазной активности наблюдается очень быстро, уже спустя 4 ч после добавления антибиотика в инфицированную культуру клеток. Для достижения равного эффекта подавления роста риккетсий требовалась большая, примерно в 2,5 раза концентрация хлорамфеникола, в сравнении с тетрациклином. Кроме того, продемонстрировано, что доксициклину, помимо этиотропного влияния, свойственно и патогенетическое действие, так как препарат также подавляет синтез производных азотной кислоты в зараженных риккетсиями клетками и тем самым оказывает противовоспалительный эффект (Agostino et al., 1998).
Таблица 6

Пенициллин, наоборот, не оказывает какого-либо влияния на фосфолипазную активность риккетсий.
Назначение тетрациклина или доксициклина в общетерапевтических дозах (2,0 г тетрациклина или 200 мг доксициклина в сутки для взрослого) при острых формах риккетсиозов, таких как эпидемический и крысиный сыпной тиф, марсельская лихорадка, лихорадка цу-цугамуши (табл. 6), японская пятнистая лихорадка и моноцитарный эрлихиоз быстро, в течение 24-72 ч, улучшает состояние больных и, соответственно, приводит к нормализации температуры тела к 36-96 ч после начала лечения с последующим полным выздоровлением. По сути дела, лечение острых риккетсиозов может быть сведено лишь к приему доксициклина (200 мг в 2 капсулах), как это и было рекомендовано ВОЗ при ликвидации большой вспышки сыпного тифа в Бурунди в 1997 году. Очевидно также, что доксициклин имеет преимущество в сравнении с другими препаратами вследствие простоты применения и невысокой стоимости при равной эффективности. Для лечения пятнистых лихорадок у детей и беременных может быть использован и джозамицин (препарат из группы макролидов), поскольку его токсичность крайне низка (Drancourt, Raoult, 1993). Широкодоступные пенициллины, хлорамфеникол, котримоксазол и некоторые макролиды (эритромицин, олетерин), хотя и проявили некоторую эффективность при лечении отдельных нозоформ, все же уступают тетрациклинам, не обеспечивая ожидаемого результата.
На примере наиболее злокачественного риккетсиоза с выраженной природной очаговостью, а именно пятнистой лихорадки Скалистых гор (ПЛСГ), наглядно прослеживается прямая связь между исходом болезни и использованным средством лечения. Если в 1935-1956 гг., т.е. до внедрения в клиническую практику препаратов, действующих на грамотрицательную микрофлору, летальность при этой инфекции составляла 22%, то в последующие годы благодаря терапии тетрациклином и хлорамфениколом, она снизилась до 3,0-7,5% (Smadel, 1959; Dalton et al., 1994), хотя и сохранялась в отдельных штатах на уровне 13%(KirklandetaL, 1992).
Риск гибели прямо коррелировал с возрастом заболевших, видом применяемого антибиотика и сроком начала специфического лечения (Krebs et al., 1994). Запоздалое назначение препарата (позднее 2-5-го дня от начала болезни) чаще всего было обусловлено ошибками в первоначальном диагнозе, вследствие атипичной клинической картины заболевания из-за отсутствия сыпи у больных (57% случаев) в момент их первого обращения к врачу и отсутствия в анамнезе указания на контакт с клещом (до 50%). Нередкое отсутствие одного из указанных кардинального для ПЛГС признака или отсутствие их обоих одновременно затрудняло диагноз болезни и, соответственно, явилось причиной задержки специфического лечения (Kirkland et al., 1992).
Кроме того, из сопоставления результатов терапии ПЛГС хлорам-фениколом и тетрациклином следует, что в группе больных, получавших лечение хлорамфениколом, летальность на 827 наблюдений составила 8,9%, тогда как в группе, леченной тетрациклином, она не превышала 1,6% на 2256 больных (Dalton et al., 1994).
Очевидно, что при подозрении на риккетсиозную этиологию лихорадочного заболевания, особенно такого как ПЛГС, лихорадка цуцугамуши, марсельская лихорадка и коксиеллез, лечение антибиотиками широкого спектра действия (тетрациклин, доксициклин, миноциклин, рифампицин) должно быть немедленным, особенно у лиц старшего возраста и ослабленных больных. При назначении антибиотиков следует также учесть то, что такая терапия при своевременном применении в первые дни болезни, по существу, является этиотропной и патогенетической одновременно; это приводит к задержке специфического антительного ответа у больного и к продукции антител на невысоком уровне, иногда ниже диагностических значений (Gray et al., 1990). Но в этом случае быстрый эффект терапии следует расценивать как косвенное доказательство риккетсиозной этиологии болезни.
Наиболее сложную и трудную проблему представляет терапия коксиеллеза и хронических форм бартонеллезов. Лечение, в частности, эндокардитов коксиеллезной этиологии и других более редких осложнений лихорадки Ку, а также хронических форм бартонеллезов остается сложным и требует настойчивой, зачастую многомесячной, комбинированной терапии. Если химиопрепарат не проникает внутрь клеток, в которых паразитирует возбудитель и не аккумулируется внутри фаголизосомы (а именно в них «укрываются» коксиеллы), то он становится неэффективным и его применение малорезультативно. Вероятно, по этой причине часть препаратов группы макролидов и аминог-ликозидов (гентамицин, эритромицин, ванкомицин), а также новые антибиотики группы фторхинолонов (норфлоксацин, пефлоксацин), характеризующиеся относительно быстрым (менее 8-10 ч) периодом полувыведения из организма человека, оказываются недостаточно эффективными для лечения коксиеллеза. Так, в сравнительном исследовании результатов терапии 111 случаев острой лихорадки Ку, протекающей в различных клинических формах, свойственной этому заболеванию (см. главу: лихорадка Ку), Spelman et al. (1982) установили, что применение в общетерапевтических дозах тетрациклина (500 мг, 4 раза в день) в течение двух недель и доксициклина (100 мг дважды в день) в течение такого же срока привело к быстрому клиническому излечению всех больных. Средняя продолжительность лихорадки после начала терапии составила 2,0 и 1,7 дня соответственно. Однако в одном случае лечения тетрациклином, одном случае терапии доксициклином у 3 больных с выявленным коксиеллезным эндокардитом полного излечения не произошло. Выздоровление этих больных наступило лишь после дальнейшего длительного приема антибиотика. Кроме того, у 425 больных развилась посткоксиеллезная астения, и часть больных этой группы получила второй дополнительный курс лечения доксициклином. Именно поэтому авторы отдают предпочтение доксициклину и рекомендовали расширить основной первоначальный курс лечения данным антибиотиком до 4 недель (Spelman et al., 1982).
Аналогичной тактики пролонгированной (не менее 21 дня) терапии доксициклином при лечении острой лихорадки Ку придерживаются и французские авторы (Musso, Raoult, 1995). По результатам терапии острой (178 наблюдений) и хронической (71 больной) лихорадки Ку, осуществляемой хлорамфениколом, макролидами, доксициклином и хинолонами, под контролем присутствия коксиелл в крови и в биопробах из пораженных тканей, авторы заключили, что укороченный курс лечения антибиотиком является клинически эффективным в отношении острой лихорадки Ку, но не приводит к освобождению организма больного от коксиелл и, следовательно, не предупреждает возможную эволюцию к хронической форме болезни. Поэтому лечение должно проводиться достаточно длительно, и в наблюдениях последних авторов терапия доксициклином продолжалась в течение трех недель для острой лихорадки Ку. Терапия же хронических форм проводилась значительно продолжительнее, настойчиво — от одного-двух месяцев до полугода и более, с ежедневным приемом комбинаций антибиотиков: доксициклин с хинолонами, доксициклин с гидрооксих-лороквином, доксициклин в сочетании с рифампицином. Эффективность лечения периодически контролировали высевами коксиелл из крови или из биоптатов тканей (Musso, Raoult, 1995). Имеются также сообщения о высокоэффективном лечении легочной формы лихорадки Ку фторхинолонами при отсутствии осложнений (Bestland et al., 1988).
Лечение эрлихиозов, независимо от видовой принадлежности возбудителя, успешно осуществляется доксициклином (Walker D., 1996). Оценка чувствительности возбудителя моноцитарного эрлихиоза человека, Е. chaffeensis, к различным антибиотикам подтвердила необоснованность эмпирического применения хлорамфеникола и, наоборот, перспективность назначения рифампицина, особенно при лечении эрлихиоза у детей и у женщин в период беременности. Минимальная ингибирующая рост эрлихий в культуре клеток концентрация доксициклина и рифампицина была менее чем 0,5 и 0,125 мг/мл соответственно, тогда как хлорамфеникол не задерживал развитие возбудителя даже при концентрации антибиотика выше 16 мг/мл (Brouqui, Raoult, 1992).
Гранулоцитарный эрлихиоз успешно излечивается тетрациклинами с возвращенияем температуры и клинического состояния больных к норме в течение 24-28 ч после приема препарата (Bakken et al., 1996).
Систематизированные данные по лечению бартонеллезов отсутствуют, либо их терапия проводилась эмпирически неадекватным химио-препаратом. Рационально обоснованная терапия этой группы заболеваний, по-видимому, должна быть основана на данных Maurin et al. (1993,1996), а также Rolainet al. (1999). Определяя чувствительность бартонелл всех видов, патогенных для человека, к антибиотикам различных классов in vitro, авторы показали, что все изоляты бартонелл были высокочувствительны к беталактамам, аминогликозидам, макролидам, тетрациклинам и рифампицину. Минимальная концентрация, подавляющая рост 90% бактерий (МП К») по отношению, например, к В. guintana, была равна 0,06-0,12 мг/мл для азитромицина, доксициклина, рифампицина и спарфлоксацина (Maurin etal., 1995). Подтвержден универсальный характер действия тетрациклинов, эритромицина, рифампицина, а также беталактамов в отношении возбудителей всех бартонеллезов. При этом отмечена широкая вариация в дозах, подавляющих рост бактерий или оказывающих бактерицидное действие (Maurin et al., 1995; Rolain et al., 1999).
Поразительный эффект своевременного применения этиотропной терапии наблюдали при лечении болезни Кариона в ее острой форме (лихорадка Оройя) в одном из отдаленных поселений в Перу, в эндемичном очаге инфекции. Прием хлорамфеникола (иные препараты отсутствовали) предупредил фатальные исходы у всех больных, получивших лечение антибиотиком, при гибели 14 из 16 заболевших, не получивших препарат (Gray et al., 1990).
Из ограниченного опыта лечения хронических форм бартонеллезов, в частности, бациллярного ангиоматоза и рецидивирующих лихорадочных состояний, обусловленных либо В. quintana, В. henselae, видно, что лечение становится успешным при длительном и настойчивом применении в течение нескольких месяцев комбинированной терапии: ципрофлоксацин (750 мг внутрь ежедневно) и рифампицин (900 мг ежедневно) до полной элиминации возбудителя из организма больных (Luccy et al., 1992; Colson et al., 1996). Совершенно очевидно, что при терапии бартонеллезов имеет значение не столько выбор антибиотика, сколько продолжительность курса лечения (Maurin et al., 1996) и выбор наиболее рациональной комбинации антибиотиков группы тетрациклинов и аминогликозидов. В частности, применение гентамицина в сочетании с доксициклином не менее чем в течение 6 недель должно защитить от бартонеллезных эндокардитов (Rolain et al., 1999).
Само собой разумеется, что этиотропная терапия антибиотиками должна быть подкреплена патогенетическими препаратами с учетом клинического состояния больного.
В заключение необходимо обратить внимание на то обстоятельство, что некоторыми французскими (Herreman, 1966; Giroud, Capponi, 1968), румынскими (Илиеску К. и др., 1962; Nicolau, Constantinescu, 1965; Стоя И. и др., 1965) и турецкими исследователями (Payzin, Akan, 1966) высказывалось предположение о возможности не только длительного паразитирования риккетсий в организме переболевших, но и о возможности развития в связи с этим у них различного рода сердечной и сосудистой патологии через многие годы после перенесенного риккетсиоза. Это детерминируется ангиотропизмом в паразитировании риккетсий, который патогистологически проявляется в виде сосудистого эндотелиоза, а в остром периоде риккетсиоза — в виде специфического риккетсиозного гранулематоза. Риккетсиям приписывается ответственность за возможность последующего развития у перенесших основной процесс миокардиокоронаритов, тромбангиитов и даже инфаркта миокарда.
Указанные выше французские и румынские исследователи считают, что такая патология может быть обусловлена риккетсиями Провачека, риккетсиями Музера, риккетсиями Конора и коксиеллами Бернета. Такого рода суждения обосновываются тем, что у больных с сердечно-сосудистой патологией иногда выявляются антитела в сыворотке крови больных к риккетсиям и даже, возможно, выделение самих риккетсий. Больше это касается коксиелл Бернета, которые являются, пожалуй, единственным видом риккетсий, способным вызывать тяжелую патологию сердца у больных лихорадкой Ку, причем не только по типу интерстициального миокардита, но даже и риккетсиозный эндокардит. Последний описан у ряда больных и, как правило, характеризуется затяжным или даже хроническим течением. Затяжное течение болезни, не свойственное другим риккетсиозам, при лихорадке Ку объясняется размножением и развитием риккетсий в гистиоцитах, а затем и в макрофагах органов (макрофагальной) ретикуло-эндотелиальной системы, в то время как при других риккетсиозах возбудители паразитируют в основном в эндотелии сосудов. Захваченные лейкоцитами, макрофагами и гистиоцитами, коксиеллы Бернета частично лизируются (в основном в лейкоцитах), но могут также и размножаться в них. Речь идет, таким образом, о том, что фагоцитоз риккетсий при лихорадке Ку имеет, в отличие от других риккетсиозов, незавершенный характер. С этим, повидимому, и следует связывать наличие субклинических форм болезни и латентно протекающей инфекции при данном риккетсиозе.
Именно латентная инфекция в последующем, по представлению указанных выше авторов, и может вести к медленному прогрессирующему процессу с развитием картины коронарита, миокардиокоронарита и ишемии миокарда. Выявление в сыворотке крови комплемент-фиксирующих антител к риккетсиям может быть косвенным подтверждением гипотезы о причастности риккетсий к патологии сердечно-сосудистой системы у переболевших когда-то лихорадкой Ку или другими риккетсиозами.